Sie befinden sich hier
Inhalt
Unser Forschungsinteresse ist die Aufklärung wesentlicher Schlüsselmechanismen der Tumormetastasierung. Hierbei interessieren wir uns insbesondere für microRNAs sowie auch tumor-assoziierte Proteasen in ihrer Eigenschaft als molekulare Regulatoren des Metastasierungsprozesses. In diesem Zusammenhang ist es nicht nur unser Anliegen, wesentliche Schlüsselmoleküle der Metastasierung und deren molekulare Netzwerke zu definieren, sondern auch in translationalen Projekten zu untersuchen. Diese haben zum Ziel abzuklären, welche dieser Schlüsselmoleküle ggf. als neue Biomarker geeignet sind, die individuelle Risikowahrscheinlichkeit eines einzelnen Patienten für die Entwicklung einer Metastasierung, eine bestimmte Art des Krankheitsverlaufs oder die Wahrscheinlichkeit für das Ansprechen auf bestimmte neue Therapieformen vorherzusagen, an einer präziseren interdisziplinären Diagnostik mitzuwirken (Stichwort: “Molekulares Tumorstaging”), und idealerweise zur Prävention von Metastasierung geeignet sein können.
Erweiterte molekulare Stagingmodelle
In der Vergangenheit beschrieben wir bereits für verschiedene Tumorentitäten gültige zentrale molekulare Mechanismen, mit denen der Urokinase-Rezeptor (u-PAR) aus dem Gebiet der tumorassoziierten Proteolyse verschiedene Schritte der Metastasierungskaskade steuert, und schlugen basierend auf transkriptionalen und onkogenen Regulatoren des u-PAR erweiterte molekulare Stagingmodelle vor, die eine präzisere individuelle Risikoklassifikation bei Patienten mit gastrointestinalen Tumoren und bei Nachweis einer minimal residualen Tumorerkrankung erlaubten. Ferner wiesen wir eine anti-metastatische Wirkung u.a. des EGFR-Inhibitors Cetuximab über eine Inhibition des u-PAR nach und schlugen u-PAR als neuen Biomarker der Therapieantwort auf Cetuximab vor. Erstmals gelang uns auch der Nachweis einer Metastasierungsinhibition durch das Anti-Malaria-Medikament Artesunat über die Hemmung des u-PAR-Liganden u-PA und verschiedener Matrix-Metalloproteinasen (MMPs).
Drei essenzielle Schritte der Metastasierungskaskade
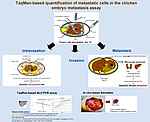
Als Brücke zur microRNA-Forschung waren wir schließlich die ersten, die nicht nur zeigten, dass der neue Tumorsuppressor Pdcd4 insbesondere über die Herunterregulation von u-PAR Tumormetastasierung hemmt, sondern insbesondere auch, dass microRNA-21 (miR-21) über die Hemmung der Translation von Pdcd4 drei essenzielle Schritte der Metastasierungskaskade (Invasion, Intravasation, Metastasierung in vivo) anregt. Dies wurde inzwischen von zahlreichen anderen Arbeitsgruppen und Arbeiten an verschiedenen Tumorentitäten bestätigt.
In jüngster Zeit konzentrierten wir uns entsprechend insbesondere auf die Definition der besonderen Funktion von microRNAs (miRs) in der Tumormetastasierung. Neben microRNA-21 als einem wesentlichen miR-Protagonisten der Metastasierung charakterisierten wir weitere spezifische miRs bzw. miR-Familien als neue positive oder negative Regulatoren der Metastasierung verschiedener Karzinome, z.B. miR-200c, miR-34a, oder die miR-30-Familie.
miR-orchestrierte molekulare Netzwerke
In unseren aktuellsten Arbeiten charakterisierten wir, zusammen mit zahlreichen nationalen und internationalen Kooperationspartnern, mehrere miR-orchestrierte molekulare Netzwerke, die für die Metastasierung von zentraler Relevanz sind, z.B. ein Netzwerk aus miR-21, miR-34a, Pdcd4, Src, und PTEN. Wir führten zudem in resezierten Metastasengeweben von kolorektalen Karzinomen eine systematische Hypothesengenerierung durch miR-Profiling im Vergleich zu den korrespondierenden Primärtumoren und Normalgeweben durch, aus der heraus wir eine metastasenspezifische Signatur und ein resultierendes erstes, mechanistisch validiertes Netzwerk aus miRs vorschlagen, das über die z.T. gemeinsame Regulation von mindestens 5 neuen Zielmolekülen den für die Metastasierung zentralen Prozess der epithelial-mesenchymalen Transition (EMT) und dadurch Invasion, Intravasation und Metastasierung in vitro und in vivo orchestriert. Unsere Arbeiten tragen aktuell auch aktiv zur Diagnostikentwicklung und Identifizierbarkeit metastatisch relevanter Einzelzellen innerhalb der Heterogenität primärer Tumorzellen bei.
So etablierten wir in einem interdisziplinären Ansatz mit Kollegen der Biophysik und des molekularen Imagings erstmals erfolgreich die Laser-Superresolutionsmikroskopie zur Sichtbarmachung einzelner humaner microRNAs auf Einzelmolekül-Einzelzell-Ebene, wobei wir Unterschiede in der subzellulären Lokalisation einzelner miRs zwischen metastatischen und nicht metastatischen Tumorzellen feststellen. In laufenden Projekten erweitern wir unsere Aktivitäten u.a. auf die Definition genetischer und epigenetischer Ursachen der miR-Deregulation im Metastasierungsprozess sowie von spezifischen molekularen Parametern der organspezifischen Metastasierung.
Systematische genomische und molekulare Charakterisierung von Metastasen - das Krebs-„Metastasom”
In jüngster Zeit widmen sich unsere wissenschaftlichen Aktivitäten zunehmend der Charakterisierung des “Big Pictures” von Metastasen, also der systematischen Identifizierung genomischer und weiterer molekularer Charakteristika , die Metastasen, oder metastatisch relevante Tumorzellen, von nicht-metastatischen Tumoren/Tumorzellen unterscheiden (Identifizierung des “Metastasoms”, ein Begriff, den wir neu geprägt haben, siehe Allgayer et al., Seminars in Cancer Biology 2020). Hierzu haben wir nicht nur vor einigen Jahren die metastatisch relevante microRNA-“Landschaft” für das colorektale Karzinom charakterisiert (Mudduluru et al., Cancer Research 2015), sondern haben kürzlich die zu diesem Zeitpunkt umfassendste Untersuchung des gesamten Genoms von Metastasen des colorektalen Karzinoms in einer translational-interdisziplinären Team-Arbeit mit vielen Beteiligten durchgeführt (Ishaque et al., Nature Communications 2018). In dieser Arbeit zeigen wir, dass Metastasen und zugehöriger Primärtumor einen gemeinsamen Ursprungsklon haben, dass sie aber im Laufe ihrer Entwicklung bereits auf Genomebene Veränderungen entwickeln, die sie von ihrem zugehörigen Primärtumor unterscheiden. Dies führte u.a. zur Definition eines neuen Progressions-und Metastasierungsmodells des colorektalen Karzinoms (Allgayer et al., Seminars in Cancer Biology 2020). Zusammen mit Arbeiten weiterer Gruppen kann dies Grundlagen für die zukünftige Entwicklung metastasen-spezifischerer Konzepte der personalisierten Diagnostik und Therapie bilden, die viel zielgerichteter auf Metastasen und deren Vermeidung ausgerichtet sind. Wir legen unseren Fokus zur Zeit konsequenterweise, in interdisziplinären Netzwerken, auf die Erarbeitung eines noch umfassenderen molekularen Verständnisses des “Metastasoms”, was insbesondere auch Arbeiten zur bisher immer noch kaum verstandenen organspezifischen Metastasierung einschließt. Unser langfristiges ultimatives Ziel ist der Beitrag zu einer neuen Ära metastasen-spezifischer Diagnostik, Therapie und, idealerweise, Metastasen-Prävention.
Prof. Dr. med. Heike Allgayer
Die Experimentelle Chirurgie und Tumormetastasierung ist Teil der Medizinischen Fakultät Mannheim der Universität Heidelberg. Prof. Dr. med. Heike Allgayer, MD, PhD, erhielt ihre ärztliche Approbation und Promotion zum Dr. med. 1995/1996 an der Ludwig-Maximilians Universität München, ihren PhD für Molekularbiologie 1999 an der University of Texas-Houston und am MD Anderson Cancer Center, Houston, USA. Als Fachärztin für Chirurgie und Molekularbiologin sieht sie unsere Mission insbesondere in der Brückenbildung zwischen Grundlagenforschung und einer möglichst zeitnahen, durch translationale Forschung unterstützten Entwicklung einer diagnostischen und therapeutischen Metastasierungsprävention für die Klinik (CV Prof. Allgayer). Innerhalb zahlreicher Aktivitäten und Assoziationen ist Frau Prof. Allgayer z. B. aktives Mitglied der AACR (American Association for Cancer Research, im Moment zusätzlich Mitglied der AACR Surgical Oncology Task Force), der American Society for Clinical Oncology (ASCO), der Metastasis Research Society (MRS), und der European Association for Cancer Research (EACR) (als Council Member und Ambassador). Ferner ist sie die Vorsitzende der Preisträgerinnen und Fellows der Ingrid zu Solms Stiftung (IzS), sowie Associate Editor des International Journal of Cancer (IJC).
Kontextspalte
Experimentelle Chirurgie & Tumormetastasierung
Medizinische Fakultät Mannheim der Universität Heidelberg
Ludolf-Krehl-Straße 13-17
68167 Mannheim
Telefon 0621 383-71630, -71635 oder -71406
Fax 0621 383-71631
experimentelle.chirurgie@medma.uni-heidelberg.de
Direktorin

Prof. Dr. med. Heike Allgayer, MD, PhD
Telefon 0621 383-71635
heike.allgayer@medma.uni-heidelberg.de