Sie befinden sich hier
Inhalt
Erbliche Thrombozytenfunktionsstörungen
Thrombozyten erfüllen ihre primäre Aufgabe im Rahmen der Hämostase (Blutstillung). Bei Gefäßverletzung werden Thrombozyten aktiviert und aggregieren zu einem primären Thrombus, was auch als zelluläre Hämostase bezeichnet wird. Durch die plasmatische Gerinnung wird schließlich der sekundäre Thrombus gebildet, der einen stabilen Verschluss der Verletzung gewährleistet. Patienten mit erworbener oder erblicher Thrombozytenfunktionsstörung (Thrombopathie) können milde bis schwere Blutungsneigungen entwickeln. Während erworbene Thrombopathien häufig immunologische Ursachen haben, sind die molekularen Pathomechanismen der erblichen Formen sehr heterogen.
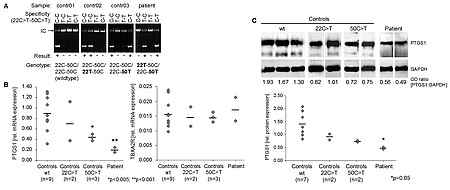
Die Arbeitsgruppe befasst sich hauptsächlich mit Defekten im Arachidonsäure-Stoffwechsel der Thrombozyten, die zum sogenannten Aspirin-like Defect (ALD). Diese seltene Thrombopathie ist mit einer milden Blutungsneigung behaftet und ist in der Labordiagnostik durch eine fehlende Aggregation der Thrombozyten nach Arachidonsäure-Stimulation gekennzeichnet. Die molekulargenetischen Ursachen sind jedoch in den meisten Fällen unklar. In selteneren Fällen konnten Genvarianten der Cyclooxygenase 1 mit dem ALD in Verbindung gebracht werden.
Aktuelle Projekte
- Charakterisierung der ADP und Thromboxan A2 Rezeptorexpression bei der ex vivo Megakaryopoiese
- Etablierung der ADP und Thromboxan A2 Rezeptor-Quantifizierung bei Gesunden und bei Patienten mit Verdacht auf Thrombopathie
Thrombozytenfunktion bei malignen und neuropsychiatrischen Erkrankungen
Aus der Grundlagenforschung und der klinischen Forschung werden zunehmend Erkenntnisse gewonnen, die eine Beteiligung der Thrombozyten an der Progression und Metastasierung solider Tumore nahelegen. Insbesondere die über verschiedene Rezeptoren vermittelten zelladhäsiven Eigenschaften der Thrombozyten scheinen hierbei von zentraler Bedeutung zu sein. Der CLEC-2 Rezeptor wird von Thrombozyten exprimiert und bindet spezifisch an Podoplanin, das unter anderem von Tumorzellen exprimiert wird. Über diese Rezeptorinteraktion binden Thrombozyten an im Blut zirkulierende Tumorzellen und erleichtern deren Anheftung an das Endothel. Dieser Mechanismus könnte die Ansiedlung von Tumorzellen und damit die Metastasierung zumindest begünstigen.
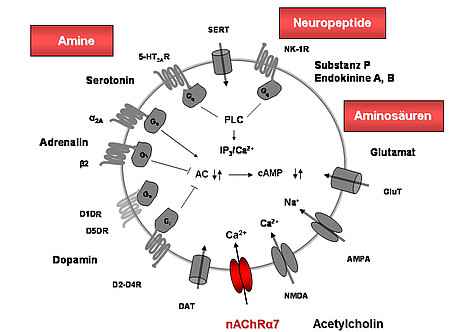
Thrombozyten und Zellen der neuronalen Gewebe zeigen erstaunliche Gemeinsamkeiten im Bezug auf die Ausstattung mit Rezeptoren und Enzymen sowie verschiedener Neurotransmitter. Bekannteste Beispiele sind die funktionellen Systeme für Serotonin, Dopamin und auch Acetylcholin.
Die Arbeitsgruppe befasst sich in Kooperation mit dem ZI Mannheim mit der Frage, ob bei Patienten mit neuropsychiatrischen bzw. neurodegenerativen Erkrankungen die Thrombozytenfunktion verändert ist und ob die Expression oder Funktion der neuronalen Moleküle in den Thrombozyten verändert ist. Aktuelle Arbeiten an Alzheimer-Patienten sollen solche Veränderungen aufzeigen und prüfen, ob Thrombozyten sich als periphere Biomarker für die Diagnose der Alzheimer-Erkrankung eignen.
Aktuelle Projekte
- Bedeutung von CLEC-2 für die ex vivo Megakaryopoiese.
- CLEC-2 Genvarianten und deren Assoziation mit dem sCLEC-2 Plasmaspiegel bei Gesunden und Tumorpatienten.
- Funktionelle und molekulare Charakterisierung der Thrombozyten bei Alzheimer-Patienten
Molekulare Genetik der humanen Blutgruppensysteme
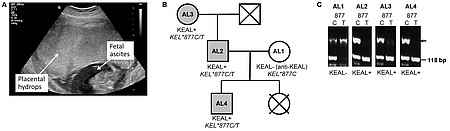
Mit der Entdeckung und Beschreibung des ABO Blutgruppenssystems durch Karl Landsteiner 1900 wurde der Grundstein für die moderne Transfusionsmedizin und Immunhämatologie gelegt. Bis heute sind 36 Blutgruppensysteme mit über 350 Antigenen beschrieben, von denen viele klinisch relevant sind. Die molekulargenetischen Grundlagen der Blutgruppensysteme konnte in den letzten Jahrzehnten ebenfalls systematisch aufgeklärt werden. Trotz dieser bereits umfassenden Kenntnisse werden immer wieder neue Blutgruppenantigene durch entsprechende klinische Fälle beschrieben. Jüngstes Beispiel ist das durch unsere Arbeitsgruppe beschriebene KEAL Antigen aus dem KEL Blutgruppensystem. Das KEAL Antigen wurde als Ursache eines schwerwiegenden Morbus Haemolyticus Neonatorum (MHN) identifiziert und beruht auf einer Punktmutation im KEL Gen.
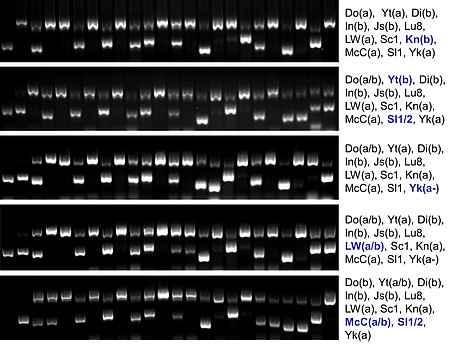
Die immunhämatologische Diagnostik wird zunehmend von den Kenntnissen der genetischen Grundlagen der Blutgruppensysteme geprägt. Neben der Antikörperdiagnostik gewinnt deshalb die Bestimmung der Blutgruppenantigene mittels molekulargenetischer Verfahren zunehmend an Bedeutung. Die Entwicklung solcher Testverfahren bildet einen wichtigen Schwerpunkt der Arbeitsgruppe.
Aktuelle Projekte
- Erweiterte Blutgruppen-Genotypisierung der Blutspender des Instituts
- Charakterisierung von ABO und RHCE Genvarianten mit auffälligem Phänotyp
- Einführung der digitalen PCR in die nichtinvasive Pränataldiagnostik von Blutgruppenantigenen
Antigene der Leukozyten
Neben der ABO Blutgruppe sind die humanen Leukozytenantigene (HLA) die wichtigsten immunologischen Merkmale im Rahmen der Transplantations- und Transfusionsmedizin. Der Erfolg einer allogenen Stammzelltransplantation hängt wesentlich von der Übereinstimmung dieser Merkmale zwischen Spender und Empfänger ab. Durch die weltweite Einrichtung von Stammzellspenderdateien wurde die allogene Stammzelltransplantation zu einer erfolgreichen Therapie in der Hämatoonkologie.
Die Transfusionsassoziierte Lungeninsuffizienz (TRALI) stellt die häufigste schwerwiegende Transfusionsreaktion dar, die in etwa 20 % der Fälle zum Tod führt. In den meisten Fällen wird die TRALI durch Antikörper des Spenders gegen HLA Merkmale aber auch gegen Antigene der neutrophilen Granulozyten (HNA, humane Neutrophilenantigene) ausgelöst. Deshalb sind insbesondere plasmareiche Blutpräparate an der Verursachung der TRALI beteiligt. Neben der Antikörperdiagnostik spielt die Kenntnis des Antigenstatus (HLA und HNA) bei Spendern und Patienten eine große Rolle. Auch beim therapeutischen Einsatz von Granulozyten (Granulozytentransfusion) ist der HLA und HNA Antigenmatch eine wichtige Voraussetzung für den Therapieerfolg.
Die Arbeitsgruppe befasst sich auf diesem Gebiet im Wesentlichen mit der Entwicklung molekulargenetischer Testverfahren zur Bestimmung der HLA und HNA Merkmale. Die funktionelle Charakterisierung von Granulozytenpräparaten stellt ein weiteres Forschungsprojekt dar.
Aktuelle Projekte
- Kooperationsprojekt zur Entwicklung eines vollintegrierten und geschlossenen Systems (Lab-on-a-Disc) zur schnellen molekulargenetischen HLA-Typisierung (HLA-Express; gefördert durch das BMBF).
- Etablierung PCR-basierter Verfahren zur molekulargenetischen Bestimmung des HNA-2 Merkmals.
- Vergleichende funktionelle Charakterisierung von Granulozytenpräparaten aus Buffy Coat und aus Apherese.
AKTUELLE PUBLIKATIONEN
- Kronstein-Wiedemann R, Nowakowska P, Milanov P, Gubbe K, Seifried E, Bugert P, Chavakis T, Tonn T. Regulation of ABO blood group antigen expression by miR-331-3p and miR-1908-5p during hematopoietic stem cell differentiation. Stem Cells. 2020 Jul 4. doi: 10.1002/stem.3251. Online ahead of print.
- Gerhards C, Uhlig S, Etemad M, Christodoulou F, Bieback K, Klüter H, Bugert P. Expression of ADP receptor P2Y12, thromboxane A2 receptor and C-type lectin-like receptor 2 in cord blood-derived megakaryopoiesis. Platelets. 2020 Jul 3:1-8. doi: 10.1080/09537104.2020.1782868. Online ahead of print.
- Scharberg EA, Rink G, Schulz D, Rothenberger S, Stürtzel A, Gillhuber N, Seyboth S, Bugert P. KDAS, a new blood group antigen in the Knops blood group system antithetical to KCAM. Transfusion. 2020 Jun 26. doi: 10.1111/trf.15938. Online ahead of print.
- Pletsch-Borba L, Grafetstätter M, Hüsing A, Johnson T, González Maldonado S, Groß ML, Kloss M, Hoffmeister M, Bugert P, Kaaks R, Kühn T. Vascular injury biomarkers and stroke risk: A population-based study. Neurology. 2020 Jun 2;94(22):e2337-e2345.
- Masamune A, Kotani H, Sörgel FL, Chen JM, Hamada S, Sakaguchi R, Masson E, Nakano E, Kakuta Y, Niihori T, Funayama R, Shirota M, Hirano T, Kawamoto T, Hosokoshi A, Kume K, Unger L, Ewers M, Laumen H, Bugert P, Mori MX, Tsvilovskyy V, Weißgerber P, Kriebs U, Fecher-Trost C, Freichel M, Diakopoulos KN, Berninger A, Lesina M, Ishii K, Itoi T, Ikeura T, Okazaki K, Kaune T, Rosendahl J, Nagasaki M, Uezono Y, Algül H, Nakayama K, Matsubara Y, Aoki Y, Férec C, Mori Y, Witt H, Shimosegawa T. Variants That Affect Function of Calcium Channel TRPV6 Are Associated With Early-onset Chronic Pancreatitis: TRPV6 and pancreatitis. Gastroenterology 2020;158:1626-1641.
- Böhme R, Becker C, Keil B, Damm M, Rasch S, Beer S, Schneider R, Kovacs P, Bugert P, Riedel J, Griesmann H, Ruffert C, Kaune T, Michl P, Hesselbarth N, Rosendahl J. Serum levels of advanced glycation end products and their receptors sRAGE and Galectin-3 in chronic pancreatitis. Pancreatology 2020;20:187-192.
- Bugert P, Fischer L, Althaus K, Knöfler R, Bakchoul T. Platelet dysfunction caused by a novel thromboxane A2 receptor mutation and congenital thrombocytopenia in a case of mild bleeding. Platelets 31: 276-279 (2020).
- Pletsch-Borba L, Watzinger C, Turzanski Fortner R, Katzke V, Schwingshackl L, Sowah SA, Hüsing A, Johnson T, Groß ML, González Maldonado S, Hoffmeister M, Bugert P, Kaaks R, Grafetstätter M, Kühn T. Biomarkers of Vascular Injury and Type 2 Diabetes: A Prospective Study, Systematic Review and Meta-Analysis. J Clin Med 8: pii: E2075 (2019).
- Kaune T, Hollenbach M, Keil B, Chen JM, Masson E, Becker C, Damm M, Ruffert C, Grützmann R, Hoffmeister A, Te Morsche RHM, Cavestro GM, Zuppardo RA, Saftoiu A, Malecka-Panas E, Głuszek S, Bugert P, Lerch MM, Weiss FU, Zou WB, Liao Z, Hegyi P, Drenth JP, Riedel J, Férec C, Scholz M, Kirsten H, Tóth A, Ewers M, Witt H, Griesmann H, Michl P, Rosendahl J: Common variants in glyoxalase I do not increase chronic pancreatitis risk. PLoS One 14:e0222927 (2019).
- Grafetstätter M, Pletsch-Borba L, Sookthai D, Karavasiloglou N, Johnson T, Katzke VA, Hoffmeister M, Bugert P, Kaaks R, Kühn T. Thrombomodulin and Thrombopoietin, Two Biomarkers of Hemostasis, Are Positively Associated with Adherence to the World Cancer Research Fund/American Institute for Cancer Research Recommendations for Cancer Prevention in a Population-Based Cross-Sectional Study. Nutrients 11: pii: E2067 (2019).
- Wiest I, Wiemers T, Kraus MJ, Neeb H, Strasser EF, Hausner L, Frölich L, Bugert P. Multivariate platelet analysis differentiates between patients with Alzheimer's disease and healthy controls at first clinical diagnosis. J Alzheimers Dis 71: 993-1004 (2019).
- Grafetstätter M, Hüsing A, González Maldonado S, Sookthai D, Johnson TS, Pletsch-Borba L, Katzke V, Hoffmeister M, Bugert P, Kaaks R, Kuehn T. Plasma Fibrinogen and sP-Selectin are associated with the risk of lung cancer in a prospective study. Cancer Epidemiol Biomarkers Prev 28: 1221-1227 (2019).
- Costa B, Eisemann T, Strelau J, Spaan I, Korshunov A, Liu HK, Bugert P, Angel P, Peterziel H. Intratumoral platelet aggregate formation in a murine preclinical glioma model depends on podoplanin expression on tumor cells. Blood Adv 3: 1092-1102 (2019).
- Weinstock C, Mytilineos J, Bugert P, Sitzmann N, Pensel E, Schrezenmeier H, Fürst D. A novel allele of the atypical chemokine receptor 1 (ACKR1) gene containing the nucleotide change c.126 T>G (p.42Glu) encodes a third Duffy blood group protein sequence antithetical to that encoding Fya and Fyb antigens. Transfusion 59: 2158-2159 (2019).
- Pletsch-Borba L, Grafetstätter M, Hüsing A, González Maldonado S, Kloss M, Groß ML, Johnson T, Sookthai D, Bugert P, Kaaks R, Kühn T.Biomarkers of vascular injury in relation to myocardial infarction risk: A population-based study. Sci Rep 9: 3004 (2019). Erratum in: Sci Rep 9: 8037 (2019).
- Lasher D, Szabó A, Masamune A, Chen JM, Xiao X, Whitcomb DC, Barmada MM, Ewers M, Ruffert C, Paliwal S, Issarapu P, Bhaskar S, Mani KR, Chandak GR, Laumen H, Masson E, Kume K, Hamada S, Nakano E, Seltsam K, Bugert P, Müller T, Groneberg DA, Shimosegawa T, Rosendahl J, Férec C, Lowe ME, Witt H, Sahin-Tóth M. Protease-Sensitive Pancreatic Lipase Variants Are Associated With Early Onset Chronic Pancreatitis. Am J Gastroenterol 114: 974-983 (2019).
- Kraft B, Lombard J, Kirsch M, Wuchter P, Bugert P, Hielscher T, Blank N, Krämer A. SMC3 protein levels impact on karyotype and outcome in acute myeloid leukemia. Leukemia 33: 795-799 (2019).
Kontextspalte
Kontakt

Prof. (apl) Dr. Peter Bugert
Telefon 06213706-9495
peter.bugert@medma.uni-heidelberg.de
Mitglieder
Mani Etemad
(Cand med.)
Catharina Gerhards
(Cand. med.)
Katharina Kemp
(BTA)
Dennis Müller
(Cand. med.)
Klara Müller
(Cand. med.)
Gabi Rink
(MTLA)
Nora Rosenberger
(Cand. med.)
Tim Wiemers
(Cand med.)
Isabella Wiest
(Cand. med.)