Sie befinden sich hier
Inhalt
Translationale Schmerzforschung
In unserer Arbeitsgruppe wird die Sensibilisierung von peripheren nozizeptiven Nervenfasern untersucht, die einen Mechanismus zur Erklärung von neuropathischem und entzündlichem chronischen Schmerz darstellt. Unsere Untersuchungen basieren auf translationalen Ansätzen, die Einzelfaserableitungen beim Patienten mit chronischen Schmerzen, beim gesunden Probanden und beim Versuchstier (Schwein) beinhalten und mit funktionellen und strukturellen Verfahren kombiniert werden, die in-vivo, ex-vivo oder in Zellkultur durchgeführt werden.
- Zelluläre Modelle an Neuronen vom Schwein
Patch-clamp, Calcium-imaging und Histochemie an Spinalganglienzellen zur Untersuchung unterschiedlicher Nozizeptorklassen. Entwicklung von in-vitro Modellen, die eine räumliche Trennung von Soma und Endigung erlauben und die Interaktion der Nervenendigungen mit nicht-neuronalen Zellen ermöglicht - In-vivo extrazelluläre Ableitungen von primären Afferenzen am Schwein
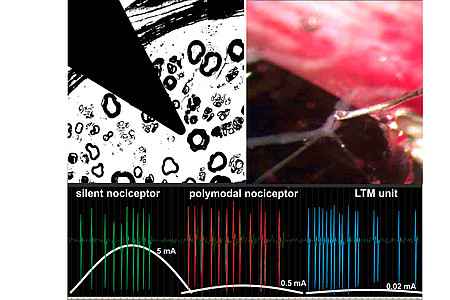
Charakterisierung von unterschiedlichen funktionellen Klassen von Nozizeptoren am Schwein anhand sensorischer und insbesondere anhand von distinkten axonalen Erregbarkeitsmustern und deren Sensibilisierung durch Wachstumsfaktoren - Sensibilisierung durch Entzündungsmediatoren
Entwicklung experimenteller Modelle zur peripheren Sensibilisierung durch UV-B Bestrahlung unter Einbeziehung objektiver Messverfahren wie z.B. Axon Reflex Erythem (laser Doppler imaging) und intradermaler Mikrodialyse - Humane Schmerzmodelle
Charakterisierung von humanen Schmerzmodellen für periphere (UVB Entzündung, Nervenwachstumsfaktor) und zentrale Sensibilisierung - Patienten mit chronischem Schmerz
Mikroneurographische Charakterisierung der Erregbarkeitsänderungen von Nozizeptorklassen bei Patienten mit neuropathischem Schmerz. Korrelation der funktionellen und strukturellen Änderungen mit Mutationen von neuronalen Ionenkanälen
Auswahl aktueller Publikationen
- Gonzalez-Rodriguez S, Quadir MA, Gupta S, Walker KA, Zhang X, Spahn V, Labuz D, Rodriguez-Gaztelumendi A, Schmelz M, Joseph J, Parr MK, Machelska H, Haag R, Stein C. Polyglycerol-opioid conjugate produces analgesia devoid of side effects. Elife 2017;6.
- Jonas R, Klusch A, Schmelz M, Petersen M, Carr RW. Assessment of TTX-s and TTX-r Action Potential Conduction along Neurites of NGF and GDNF Cultured Porcine DRG Somata. PLoS ONE 2015;10(9):e0139107.
- Jonas R, Namer B, Stockinger L, Chisholm K, Schnakenberg M, Landmann G, Kucharczyk M, Konrad C, Schmidt R, Carr R, McMahon S, Schmelz M, Rukwied R. Tuning in C-nociceptors to reveal mechanisms in chronic neuropathic pain. Ann Neurol 2018;83(5):945-957.
- Jonas R, Prato V, Lechner SG, Groen G, Obreja O, Werland F, Rukwied R, Klusch A, Petersen M, Carr RW, Schmelz M. TTX-Resistant Sodium Channels Functionally Separate Silent From Polymodal C-nociceptors. Frontiers in Cellular Neuroscience 2020;14(13).
- Klusch A, Gorzelanny C, Reeh PW, Schmelz M, Petersen M, Sauer SK. Local NGF and GDNF levels modulate morphology and function of porcine DRG neurites, In Vitro. PLoS ONE 2018;13(9):e0203215.
- Namer B, Orstavik K, Schmidt R, Kleggetveit IP, Weidner C, Mork C, Kvernebo MS, Kvernebo K, Salter H, Carr TH, Segerdahl M, Quiding H, Waxman SG, Handwerker HO, Torebjork HE, Jorum E, Schmelz M. Specific changes in conduction velocity recovery cycles of single nociceptors in a patient with erythromelalgia with the I848T gain-of-function mutation of Nav1.7. Pain 2015;156(9):1637-1646.
- Obreja O, Rukwied R, Nagler L, Schmidt M, Schmelz M, Namer B. Nerve growth factor locally sensitizes nociceptors in human skin. Pain 2018;159(3):416-426.
- Sauerstein K, Liebelt J, Namer B, Schmidt R, Rukwied R, Schmelz M. Low-Frequency Stimulation of Silent Nociceptors Induces Secondary Mechanical Hyperalgesia in Human Skin. Neuroscience 2018;387:4-12.
- Steinhoff M, Schmelz M, Szabo IL, Oaklander AL. Clinical presentation, management, and pathophysiology of neuropathic itch. Lancet Neurol 2018;17(8):709-720.
- Yosipovitch G, Greaves MW, Schmelz M. Itch. The Lancet 2003;361(9358):690-694.
Kontextspalte
Kontakt

Prof. Dr. Martin Schmelz
Experimentelle Schmerzforschung
Medizinische Fakultät Mannheim
Universität Heidelberg
Ludolf-Krehl-Str. 13-17
68167 Mannheim
Telefon 0621 383-71650
martin.schmelz@medma.uni-heidelberg.de
