Sie befinden sich hier
Inhalt
Ziel der physikalisch/methodischen Forschungsarbeiten im Bereich der medizinischen Bildgebung ist es, innovative Diagnosemethoden und Verfahren zu entwickeln, um die morphologische, funktionelle und metabolische Diagnostik zu optimieren. Dies dient als Grundlage für die Radiologie, Interventionelle Radiologie, Nuklearmedizin und bildgestützte Strahlentherapie.
Neben einer experimentellen, klinisch-translationalen Forschung an einem hochauflösenden Tiergeräts bei 9.4 Tesla soll parallel in Zukunft die Translation dieser Ergebnisse in die klinische Forschung etabliert werden. Dazu werden derzeit Anstrengungen zur Beschaffung eines klinischen 7 Tesla MRTs unternommen, um entsprechende Forschungsaktivitäten auf dem Gebiet der Hochfeld-MRT zu etablieren.
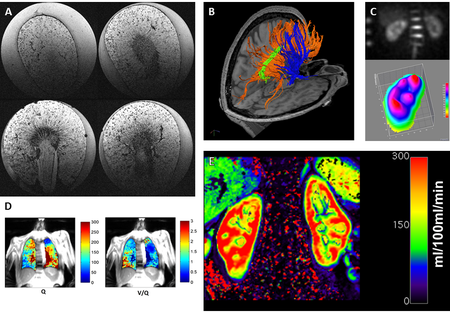
Im Fokus der laufenden Entwicklungsarbeiten stehen Methoden zur physiologischen, quantitativen MR-Bildgebung (Perfusion, Diffusion, Oxygenierung, etc.), sowie die 23Na-Bildgebung zur nicht-invasiven Messung der Gewebevitalität. Neben den Bildgebungstechniken wird zudem an Methoden und Techniken für eine Quantifizierung der Bildinformation geforscht und in Zusammenarbeit mit der Radiologie zu in-house zertifizierter Software weiterentwickelt und somit in die klinische Routine überführt (siehe Open Source Software Plattform OpossUMM).
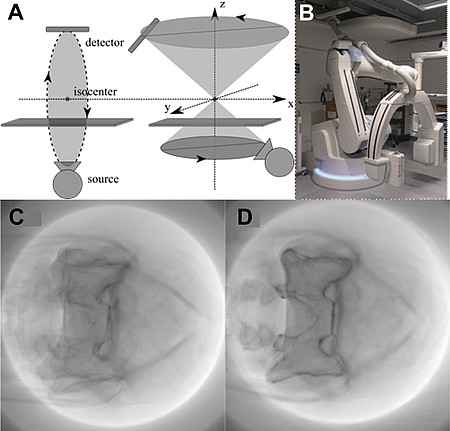
Im Bereich CT zielen Forschungsarbeiten auf neue intelligente Aufnahmetechniken, z. B. Techniken mit reduzierter Dosis oder 4D-Verfahren, die Vorwissen nutzen, um die bildgestützte, minimal-invasive Intervention zu optimieren. Diese Forschung ist eng an den Forschungscampus M2OLIE angelehnt.
Radiomics & Tracing
Moderne Bildgebungsverfahren können viel mehr als nur ein Schwarz/Weiß-Bild von Organen und Knochen zu erzeugen. Die aktuellen Verfahren sind dazu imstande, neben funktionellen auch molekulare Informationen nicht-invasiv zu gewinnen. Hierfür können zum Einen spezielle Kontrastmittel (Tracer) entwickelt werden oder zum Anderen über eine Kreuzkorrelation von Bilddaten mit klinisch-chemischen oder pathologischen Parametern Rückschlüsse auf die molekularen Eigenschaften der Gewebe (zum Beispiel von Tumoren) gewonnen werden. Die so erhaltenen Daten können erhebliche Auswirkungen auf Behandlungsstrategien, Prognose und Therapieoptionen haben und sind daher von allerhöchsten klinischen Interesse.
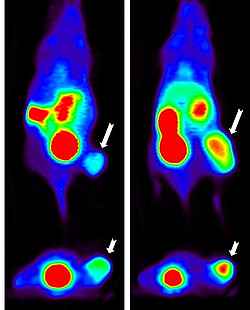
Im Bereich der Tracerentwicklung liegt der Schwerpunkt bei uns auf der Entwicklung von Target-spezifischen Radiotracern für die Positronen-Emissions-Tomographie, da die PET das sensitivste Verfahren für die funktionelle molekulare Bildgebung darstellt und auch hier die Entwicklung from-bench-to-bedside – also von der Laborbank in die klinische Anwendung – aufgrund der ultrakleinen Stoffmengen, die für die Bildgebung notwendig sind (praktisch keine Nebenwirkungen möglich), am schnellsten erreicht werden kann. Dennoch müssen natürlich bei der Translation in die Klinik alle Vorgaben des Arzneimittelgesetzes eingehalten werden, weshalb an der UMM ein voll GMP-konformes („Gute Herstellungspraxis“) Labor etabliert wurde.
Im Bereich der Grundlagenforschung werden allerdings auch für andere Bildgebungsverfahren (Fluoreszenzbildgebung (FLI), Einzelphotonentomographie (SPECT) und Magnetresonanztomographie (MRT) neue Kontrastmittel entwickelt, synthetisiert und evaluiert.
Radiomics beruht andererseits auf dem Vergleich von klinischen Daten mit klinisch chemischen und pathologischen Ergebnissen. Die Idee hierbei ist es, aus den Bildern direkt diese molekularen Eigenschaften ableiten zu können, ohne dass zusätzliche Untersuchungen notwendig sind, was Entscheidungsprozesse und Diagnosen erheblich beschleunigt. Da diese Informationen jedoch nicht direkt (wie beim PET oder SPECT) aus den Bildern ableitbar sind, basiert Radiomics auf dem Vergleich eines einzelnen Datensatzes mit den Daten großer Patientenkollektive. Hierfür müssen die Zusammenhänge zwischen Bildinformation und molekularer Information durch Deep Learning Verfahren gefunden und klinisch etabliert werden.
Kontextspalte
Ansprechpartner

Prof. Dr. Lothar Schad
Lehrstuhl für Computerunterstützte Klinische Medizin
Medizinische Fakultät Mannheim
Haus 3, Ebene 4
Theodor-Kutzer-Ufer 1-3
68167 Mannheim
Telefon 0621 383-5121
lothar.schad@medma.uni-heidelberg.de
Ansprechpartner

Prof. Dr. Stefan Schönberg
Klinik für Radiologie und Nuklearmedizin
Medizinische Fakultät Mannheim
Haus 5, Ebene 2
Theodor Kutzer-Ufer 1-3
68167 Mannheim
Telefon 0621 383-2276
stefan.schoenberg@medma.uni-heidelberg.de
Ansprechpartner

Prof. Dr. Björn Wängler
AG Molekulare Bildgebung & Radiochemie
Universitätsmedizin Mannheim
Theodor-Kutzer-Ufer 1-3
68167 Mannheim
Telefon 0621 383-2067
bjoern.waengler@medma.uni-heidelberg.de